16/06/2025
En el corazón de la química industrial moderna, donde se forjan desde combustibles hasta productos farmacéuticos, residen los catalizadores. Estas sustancias extraordinarias son mucho más que meros aceleradores de reacciones; son los arquitectos de la eficiencia, los guardianes de la sostenibilidad y los facilitadores de procesos que, de otro modo, serían inviables o prohibitivamente costosos. Su habilidad para reducir la energía de activación necesaria para una reacción permite que los procesos químicos se desarrollen a temperaturas y presiones más bajas, lo que se traduce en un menor consumo de energía y una significativa reducción de costos. Comprender la diversidad de catalizadores y los factores que afectan su rendimiento es fundamental para optimizar la producción y avanzar hacia un futuro más verde.
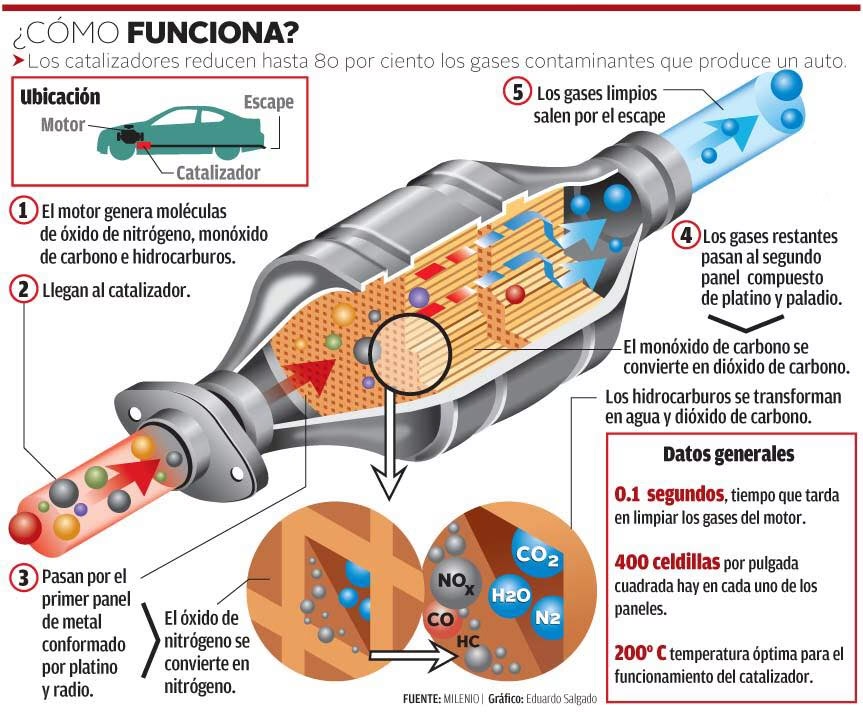
Los catalizadores no se consumen durante la reacción ni alteran la composición de equilibrio; simplemente ofrecen una vía alternativa con una energía de activación menor. Esta propiedad es clave para su papel indispensable en la industria. Su impacto se extiende más allá de la mera velocidad de reacción, influyendo profundamente en la eficiencia energética, la reducción de residuos, la producción de combustibles más limpios y el reciclaje químico, pilares fundamentales del desarrollo sostenible.
- El Papel de los Catalizadores en el Desarrollo Sostenible
- Tipos de Catalizadores Utilizados en la Química Industrial
- Comparación de Tipos de Catalizadores
- Mecanismos de Acción Catalítica: Una Mirada Más Profunda
- El Impacto del Deterioro Físico del Catalizador
- Factores Clave que Afectan la Eficacia del Catalizador
- Aplicaciones Industriales y el Futuro de los Catalizadores
- Preguntas Frecuentes (FAQ)
- ¿Cuál es la diferencia principal entre un catalizador homogéneo y uno heterogéneo?
- ¿Por qué es importante el Principio de Sabatier en la catálisis heterogénea?
- ¿Cómo contribuyen los catalizadores al desarrollo sostenible?
- ¿Qué es el envenenamiento de catalizadores y cómo difiere del deterioro físico?
- ¿Se pueden regenerar los catalizadores?
El Papel de los Catalizadores en el Desarrollo Sostenible
La búsqueda de un futuro más sostenible ha elevado el perfil de los catalizadores a un nivel de importancia sin precedentes. Su capacidad para promover reacciones químicas más eficientes, limpias y seguras los convierte en aliados cruciales para alcanzar los objetivos de desarrollo sostenible globales. A continuación, exploraremos algunas de las contribuciones más significativas:
Eficiencia Energética
Los catalizadores son fundamentales para mejorar la eficiencia de los procesos de conversión de energía. Un ejemplo claro es la producción de hidrógeno combustible a partir de agua mediante electrólisis. Catalizadores como el platino o el iridio disminuyen drásticamente la energía requerida para dividir las moléculas de agua, haciendo que este proceso sea más rentable y energéticamente eficiente. Esto es vital para la transición hacia fuentes de energía renovables y una economía basada en el hidrógeno.
Reducción de Residuos
La minimización de residuos es otro ámbito donde los catalizadores brillan. Considere la producción de botellas de tereftalato de polietileno (PET). Tradicionalmente, se usa trióxido de antimonio, un catalizador tóxico y difícil de eliminar. Sin embargo, el desarrollo de catalizadores alternativos como el circonio y el estaño, menos tóxicos y más fáciles de reciclar, ha reducido significativamente el impacto ambiental de la producción de PET, promoviendo una economía más circular.
Combustibles más Limpios
La producción de combustibles con menor impacto ambiental también depende de los catalizadores. El gas natural y el propano, que emiten menos contaminantes que los combustibles fósiles tradicionales, se convierten en formas líquidas transportables gracias a la acción de catalizadores como el níquel o el platino. Esto contribuye directamente a la reducción de la contaminación del aire y las emisiones de gases de efecto invernadero, mejorando la calidad de vida y mitigando el cambio climático.
Reciclaje Químico
El reciclaje de plásticos y otros materiales es esencial para reducir la cantidad de residuos en los vertederos. El reciclaje químico descompone los plásticos en sus componentes básicos, que luego pueden ser reutilizados para producir nuevos materiales. Los catalizadores aceleran este proceso, haciéndolo más eficiente y económicamente viable. Por ejemplo, se han desarrollado catalizadores capaces de descomponer el polietileno, uno de los plásticos más comunes, permitiendo su reutilización y cerrando el ciclo de vida de los materiales.
Tipos de Catalizadores Utilizados en la Química Industrial
La elección del catalizador en la industria depende de la reacción específica, las condiciones operativas (temperatura, presión) y el resultado deseado. Aunque existen muchas clasificaciones, nos centraremos en los tipos más comunes:
Catalizadores Homogéneos
Estos catalizadores se encuentran en la misma fase que los reactivos y productos, típicamente en solución líquida. Son solubles en la mezcla de reacción y a menudo forman complejos intermedios con los reactivos. Su principal ventaja es la alta selectividad y eficiencia, ya que pueden interactuar uniformemente con todas las moléculas reactivas. Sin embargo, su separación de la mezcla de reacción puede ser compleja y costosa, lo que puede generar problemas ambientales si no se gestionan adecuadamente. Ejemplos incluyen ácidos, bases y complejos de metales de transición.
Catalizadores Heterogéneos
A diferencia de los homogéneos, los catalizadores heterogéneos existen en una fase diferente a la de los reactivos y productos, generalmente como un sólido en contacto con fases gaseosas o líquidas. Se utilizan comúnmente en reacciones en fase gaseosa o líquida con un soporte catalítico sólido. Su principal ventaja es la facilidad de separación de la mezcla de reacción, lo que los hace más respetuosos con el medio ambiente. Sin embargo, pueden presentar menor selectividad y actividad en comparación con los homogéneos debido a la heterogeneidad de su superficie y las limitaciones de transporte de masa. Ejemplos incluyen catalizadores metálicos (platino, paladio) y óxidos metálicos (dióxido de titanio, zeolitas).
Enzimas (Biocatalizadores)
Las enzimas son biocatalizadores naturales que desempeñan un papel vital en una amplia gama de procesos industriales, desde la producción de alimentos hasta la síntesis farmacéutica. Son altamente selectivas y eficientes, y pueden operar en condiciones suaves (bajas temperaturas y presiones), lo que las hace atractivas para la química verde. Aunque pueden ser costosas y sensibles a las condiciones ambientales, su inmovilización en soportes sólidos mejora su estabilidad y facilita su separación, ampliando sus aplicaciones industriales.
Fotocatalizadores
Los fotocatalizadores son catalizadores que se activan con la luz. Se utilizan para promover diversas reacciones químicas, como la división fotocatalítica del agua para la producción de hidrógeno o la purificación fotocatalítica del aire para eliminar contaminantes. Suelen ser heterogéneos e incluyen óxidos metálicos como el dióxido de titanio o semiconductores como el óxido de silicio o zinc. Su uso puede verse limitado por la necesidad de una fuente de luz y el potencial de fotocorrosión.
Biocatalizadores (Microorganismos)
Aunque el término "biocatalizadores" a menudo se usa indistintamente con enzimas, también puede referirse a microorganismos completos que catalizan reacciones en un sistema biológico. Se emplean en aplicaciones industriales como la producción de plásticos biodegradables o la conversión de biomasa en biocombustibles. Ofrecen alta selectividad y eficiencia en condiciones suaves, pero su uso puede estar limitado por la necesidad de un sistema biológico específico y la posibilidad de contaminación microbiana.
Comparación de Tipos de Catalizadores
| Tipo de Catalizador | Fase | Ventajas | Desventajas | Ejemplos Comunes |
|---|---|---|---|---|
| Homogéneo | Misma fase (líquida, gaseosa) | Alta selectividad y actividad, contacto uniforme | Dificultad de separación, problemas ambientales | Ácidos, bases, complejos de metales de transición |
| Heterogéneo | Fase diferente (sólido) | Fácil separación, estabilidad térmica | Menor selectividad y actividad, limitaciones de transporte | Platino, Paladio, Óxidos metálicos, Zeolitas |
| Enzimas | Solución (a menudo inmovilizada) | Alta selectividad y eficiencia, condiciones suaves | Costo, sensibilidad ambiental, estabilidad | Amilasas, Lipasas, Proteasas |
| Fotocatalizadores | Fase diferente (sólido) | Activación por luz, reacciones sostenibles | Necesidad de luz, fotocorrosión | Dióxido de titanio, Óxido de zinc |
| Biocatalizadores (microorganismos) | Sistema biológico | Alta selectividad, condiciones suaves | Necesidad de sistema biológico, contaminación | Levaduras, Bacterias |
Mecanismos de Acción Catalítica: Una Mirada Más Profunda
Los catalizadores no son simplemente "cosas" que se añaden a una reacción; operan a través de mecanismos sofisticados que involucran interacciones a nivel molecular. Comprender estos mecanismos es clave para diseñar catalizadores más efectivos.

Catálisis Homogénea
En la catálisis homogénea, el catalizador entra directamente en la reacción química, formando un compuesto o complejo intermedio con un reactivo, y luego se libera en su forma original. Un ejemplo clásico es la isomerización cis-trans catalizada por yodo, donde el yodo rompe temporalmente el doble enlace, permitiendo la rotación y la posterior formación de la isomería deseada. La catálisis ácido-base, común en la química orgánica, implica la adición o eliminación de un protón, haciendo que el reactivo sea más lábil cinéticamente. Las reacciones de oxidación-reducción también pueden ser catalizadas por iones de metales de transición que alternan entre dos estados de oxidación, como el cobre en la reducción de Fe3+ por V3+.
Catálisis Heterogénea: La Importancia de la Superficie
La catálisis heterogénea se basa en la interacción de los reactivos con la superficie del catalizador. Este proceso comienza con la adsorción, donde las moléculas gaseosas o líquidas se adhieren a la superficie sólida. Se distinguen dos tipos de adsorción:
- Fisisorción: Implica fuerzas débiles de van der Waals, con poco efecto en la estructura electrónica de la molécula. Es similar a la condensación.
- Quimisorción: Implica la formación de un enlace químico entre el adsorbato y la superficie. Esta interacción "activa" la molécula, haciéndola susceptible a la reacción química, a menudo disociándola. La quimisorción es crucial para la catálisis.
Los mecanismos en superficies incluyen la adsorción disociativa, como la del hidrógeno en metales de transición, donde el hidrógeno se disocia en átomos individuales que migran sobre la superficie. Los mecanismos de reacción pueden ser:
- Langmuir-Hinshelwood: Ambas especies reactivas se adsorben en la superficie antes de reaccionar entre sí.
- Eley-Rideal: Una especie se adsorbe en la superficie y reacciona directamente con otra especie que se encuentra en la fase fluida (gas o líquido).
El Principio de Sabatier, a menudo llamado el principio de "Ricitos de Oro", es fundamental en la catálisis heterogénea. Establece que un catalizador óptimo debe tener una fuerza de adsorción "justa": lo suficientemente fuerte para activar los reactivos, pero no tan fuerte como para retener los productos e impedir su desorción, liberando así los sitios activos para el siguiente ciclo. Esto se ilustra con los "diagramas volcánicos" que muestran la tasa de reacción en función de la fuerza de adsorción.
El Impacto del Deterioro Físico del Catalizador
Aunque los catalizadores no se consumen en la reacción, su rendimiento no es eterno. En la práctica industrial, diversos factores pueden limitar su vida útil. El deterioro físico del catalizador es una de las principales causas de su pérdida de actividad y longevidad, y es crucial para la operación y economía de los procesos industriales.
Las consecuencias del deterioro físico se manifiestan de varias maneras:
- Reducción de la Superficie Efectiva: Muchos catalizadores heterogéneos dependen de una gran área superficial para su actividad. El deterioro físico, a menudo causado por altas temperaturas, puede provocar el sinterizado o la coalescencia de las partículas catalíticas. Esto reduce drásticamente el área superficial disponible para la adsorción de reactivos, disminuyendo la velocidad de reacción.
- Pérdida de Sitios Activos: Las irregularidades microscópicas, como escalones, esquinas o defectos en la superficie del catalizador, son a menudo los sitios más activos. El estrés térmico o mecánico puede alterar esta topografía superficial, eliminando o modificando estos sitios críticos. Esto se traduce en una menor cantidad de puntos donde la reacción puede ocurrir eficientemente.
- Reducción de la Accesibilidad de los Reactivos: En catalizadores porosos, como las zeolitas o los que tienen soportes, el deterioro físico puede obstruir o colapsar los canales y poros. Esto dificulta la difusión de los reactivos hacia los sitios activos internos y la salida de los productos, haciendo que el proceso sea limitado por la transferencia de masa en lugar de la cinética de la reacción.
- Fragmentación y Desintegración: El estrés repetido, los ciclos de temperatura o la abrasión pueden causar la fragmentación del catalizador o la desintegración de su soporte. Las partículas más pequeñas pueden lixiviarse o arrastrarse con el flujo de proceso, llevando a la pérdida de material catalítico y a la posible contaminación de los productos o equipos aguas abajo.
- Disminución de la Selectividad: A veces, el deterioro físico no solo reduce la actividad general, sino que también altera la selectividad del catalizador. Esto significa que el catalizador podría empezar a favorecer la formación de subproductos no deseados, lo que reduce el rendimiento del producto principal y aumenta los costos de purificación.
- Necesidad de Reemplazo o Regeneración: El deterioro físico inevitablemente lleva a la necesidad de reemplazar el catalizador gastado o de someterlo a procesos de regeneración. Dado que los catalizadores suelen ser costosos, esto representa una parte significativa de los costos operativos en la industria. El cierre periódico de las unidades de proceso para el cambio de catalizador también implica pérdidas de producción.
Es importante diferenciar el deterioro físico del "envenenamiento" del catalizador. El envenenamiento se refiere a la unión irreversible de impurezas o subproductos a los sitios activos, mientras que el deterioro físico es un cambio estructural que afecta la disponibilidad o la naturaleza de esos sitios, a menudo debido a factores térmicos o mecánicos intrínsecos al funcionamiento del reactor.
Factores Clave que Afectan la Eficacia del Catalizador
Más allá de la química intrínseca, la eficacia de un catalizador heterogéneo está fuertemente influenciada por su estructura física:
- Área de Superficie Activa: Cuanto mayor sea el área superficial expuesta a los reactivos, más sitios activos estarán disponibles. Los catalizadores se diseñan con porosidad y estructuras que maximizan esta área, a menudo depositando metales finamente divididos sobre soportes inertes.
- Topografía Superficial: Incluso las superficies aparentemente lisas poseen defectos como escalones y esquinas. Estos sitios son a menudo más reactivos y pueden ser los únicos puntos donde la catálisis ocurre eficientemente. La estabilidad de estos defectos es crucial para la longevidad del catalizador.
- Factores Estéricos: La forma y el espaciamiento de los sitios activos en la superficie deben ser compatibles con la geometría de las moléculas reactivas. Una "concordancia" estérica adecuada permite que los enlaces superficiales se formen sin distorsión significativa, facilitando la reacción.
Aplicaciones Industriales y el Futuro de los Catalizadores
Los catalizadores son la columna vertebral de innumerables procesos industriales, desde la refinación de petróleo hasta la producción de plásticos, fertilizantes y productos farmacéuticos. La investigación continua se centra en el desarrollo de catalizadores más eficientes, selectivos y sostenibles, capaces de operar en condiciones más suaves y con menor impacto ambiental. La nanotecnología ha abierto nuevas vías para diseñar catalizadores con propiedades superficiales y estructurales a medida, como los catalizadores de conglomerados metálicos o las zeolitas, que ofrecen una selectividad por tamaño y una eficiencia excepcionales. El futuro de la industria química dependerá en gran medida de la innovación en el diseño y la gestión de estos increíbles agentes de cambio.
Preguntas Frecuentes (FAQ)
¿Cuál es la diferencia principal entre un catalizador homogéneo y uno heterogéneo?
La diferencia principal radica en la fase. Un catalizador homogéneo está en la misma fase (líquida o gaseosa) que los reactivos, mientras que un catalizador heterogéneo se encuentra en una fase diferente (generalmente sólida) a la de los reactivos. Los homogéneos ofrecen alta selectividad pero son difíciles de separar; los heterogéneos son más fáciles de separar pero pueden tener menor selectividad y actividad debido a la difusión.
¿Por qué es importante el Principio de Sabatier en la catálisis heterogénea?
El Principio de Sabatier es crucial porque establece que la fuerza de unión entre el catalizador y los reactivos debe ser "justa". Si la unión es demasiado débil, los reactivos no se activarán; si es demasiado fuerte, los productos no se desorberán, bloqueando los sitios activos. Este equilibrio es fundamental para que el catalizador funcione de manera eficiente y continua.
¿Cómo contribuyen los catalizadores al desarrollo sostenible?
Los catalizadores contribuyen a la sostenibilidad al permitir reacciones más eficientes energéticamente (reduciendo el consumo de energía), minimizando la generación de residuos (mediante procesos más limpios y selectivos), facilitando la producción de combustibles menos contaminantes y promoviendo el reciclaje químico de materiales, lo que reduce la dependencia de recursos vírgenes y la acumulación de desechos.
¿Qué es el envenenamiento de catalizadores y cómo difiere del deterioro físico?
El envenenamiento de catalizadores es la pérdida de actividad debido a la unión irreversible de impurezas (como azufre o metales pesados) a los sitios activos del catalizador. El deterioro físico, en cambio, se refiere a cambios estructurales en el catalizador (como sinterizado, colapso de poros o fragmentación) que reducen su área superficial efectiva o la accesibilidad de los sitios activos, a menudo causados por altas temperaturas o estrés mecánico. Ambos resultan en una pérdida de eficiencia, pero por mecanismos diferentes.
¿Se pueden regenerar los catalizadores?
Sí, muchos catalizadores industriales pueden ser regenerados para restaurar su actividad. Los métodos de regeneración varían según el tipo de deterioro. Para el envenenamiento o la acumulación de coque, a menudo se utilizan tratamientos térmicos o químicos para eliminar las impurezas. Para el deterioro físico, como el sinterizado, la regeneración es más difícil y a veces imposible, lo que lleva al reemplazo del catalizador. La capacidad de regeneración es un factor importante en el diseño y la economía de los procesos catalíticos.
Si quieres conocer otros artículos parecidos a Catalizadores Industriales: Tipos y Durabilidad puedes visitar la categoría Acero Inoxidable.
