15/06/2022
En el corazón de muchas de las tecnologías que impulsan nuestro mundo moderno, desde los teléfonos móviles hasta los vehículos eléctricos, se encuentra un proceso químico fundamental conocido como la reacción de reducción-oxidación, o simplemente redox. Pero no todas las reacciones redox son iguales. Algunas son forzadas, requiriendo un aporte de energía, mientras que otras son inherentemente energéticas, liberando su potencia de forma natural. Es precisamente este último tipo, la reacción redox espontánea, el que nos interesa hoy.
Una reacción redox espontánea es un proceso que ocurre sin la necesidad de una entrada de energía externa, es decir, está termodinámicamente favorecido. Cuando esta reacción se diseña y controla adecuadamente, como sucede en una pila o célula galvánica, se convierte en una fuente invaluable de energía. Aquí, la energía química inherente a los reactivos se transforma directamente en energía eléctrica, un fenómeno que ha revolucionado nuestra capacidad de alimentar dispositivos y sistemas de todo tipo.
- Fundamentos de las Reacciones Redox Espontáneas
- La Pila Galvánica: El Corazón del Proceso Redox Espontáneo
- ¿Cómo Predecir la Espontaneidad de una Reacción Redox?
- Pila Galvánica vs. Celda Electrolítica: Un Contraste Esencial
- Aplicaciones Cotidianas de las Reacciones Redox Espontáneas
- Factores que Influyen en la Espontaneidad Redox
- Preguntas Frecuentes (FAQs)
Fundamentos de las Reacciones Redox Espontáneas
Para comprender qué es el redox espontáneo, primero debemos recordar los conceptos básicos de una reacción redox. Estas reacciones implican la transferencia de electrones entre dos especies químicas. Una especie se oxida (pierde electrones), y la otra se reduce (gana electrones). Ambos procesos ocurren simultáneamente; no puede haber oxidación sin reducción, y viceversa.
- Oxidación: Es la pérdida de electrones, lo que resulta en un aumento del estado de oxidación de un átomo o ion.
- Reducción: Es la ganancia de electrones, lo que resulta en una disminución del estado de oxidación de un átomo o ion.
Cuando decimos que una reacción redox es espontánea, nos referimos a que, dadas las condiciones adecuadas, la reacción procederá por sí misma hasta alcanzar el equilibrio, liberando energía en el proceso. En términos termodinámicos, esto se asocia con un cambio negativo en la energía libre de Gibbs (ΔG < 0). Cuanto más negativo sea el valor de ΔG, mayor será la fuerza impulsora y, por lo tanto, más espontánea será la reacción. Esta energía liberada puede ser calor (en reacciones exotérmicas) o, en el caso de las pilas galvánicas, energía eléctrica.
La Pila Galvánica: El Corazón del Proceso Redox Espontáneo
La pila galvánica, también conocida como celda voltaica, es el dispositivo que ingeniosamente aprovecha la energía liberada por una reacción redox espontánea para generar corriente eléctrica. Su diseño es fundamental para separar las dos “medias reacciones” (oxidación y reducción) y dirigir el flujo de electrones a través de un circuito externo. Al separar físicamente estas dos semireacciones, se obliga a los electrones a viajar a través de un conductor externo, creando así una corriente eléctrica.
Componentes Clave de una Pila Galvánica Típica:
- Ánodo: Es el electrodo donde ocurre la oxidación. Aquí, los átomos del material del electrodo pierden electrones y se disuelven en la solución como iones, o los iones en la solución pierden electrones. Los electrones liberados fluyen hacia el circuito externo. En una pila galvánica, el ánodo es el polo negativo, ya que es la fuente de electrones. Por ejemplo, en una pila de Daniell (zinc-cobre), el zinc metálico se oxida a iones zinc (Zn → Zn²⁺ + 2e⁻).
- Cátodo: Es el electrodo donde ocurre la reducción. Los electrones que viajan desde el ánodo a través del circuito externo son consumidos aquí por iones en la solución, que se depositan como metal en el electrodo, o por el material del propio electrodo. En una pila galvánica, el cátodo es el polo positivo. En la pila de Daniell, los iones cobre (Cu²⁺) en solución se reducen a cobre metálico (Cu²⁺ + 2e⁻ → Cu).
- Electrolitos: Son las soluciones iónicas en las que se sumergen los electrodos. Estas soluciones deben contener iones que puedan participar en las reacciones redox o que puedan moverse libremente para mantener la neutralidad de carga en cada semicelda.
- Circuito Externo: Un conductor (generalmente un cable) que conecta el ánodo y el cátodo, proporcionando una ruta para que los electrones fluyan desde el ánodo (donde se producen) hacia el cátodo (donde se consumen). Este flujo de electrones constituye la corriente eléctrica que podemos aprovechar.
- Puente Salino: Un componente crucial, generalmente un tubo en forma de U invertida que contiene una solución de sal inerte (como KNO₃ o KCl) o un gel conductor. Su función es permitir el flujo de iones entre las dos semiceldas para mantener la neutralidad de carga. A medida que el ánodo produce iones positivos y el cátodo consume iones positivos (o produce iones negativos), el puente salino suministra iones para compensar estos cambios, evitando una acumulación de carga que detendría rápidamente el flujo de electrones y, por ende, la reacción.
El potencial eléctrico (voltaje) generado por una pila galvánica depende de la diferencia en la "tendencia" de cada electrodo a ganar o perder electrones, lo que se conoce como potencial de electrodo. Cuanto mayor sea esta diferencia, mayor será el voltaje que la pila puede producir de manera eficiente.
¿Cómo Predecir la Espontaneidad de una Reacción Redox?
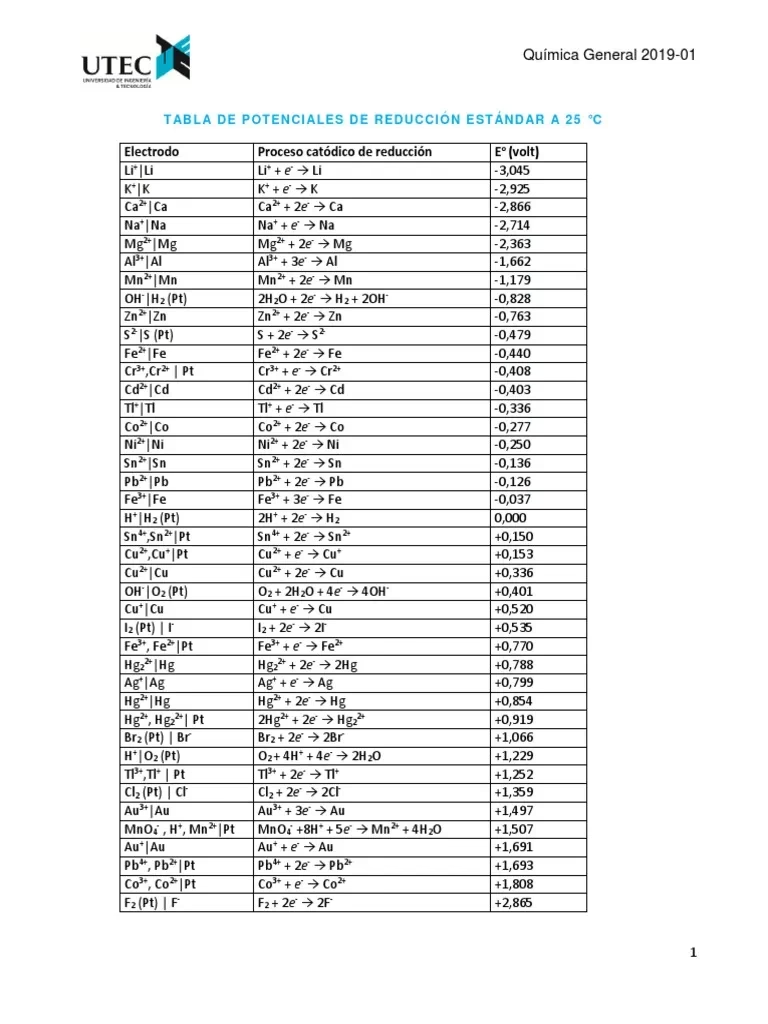
La espontaneidad de una reacción redox, y por lo tanto, la capacidad de una pila galvánica para generar electricidad, puede predecirse utilizando los potenciales estándar de reducción (E°). Estos valores tabulados representan la tendencia relativa de una especie a ser reducida bajo condiciones estándar (25°C, 1 atmósfera de presión para gases, 1 M de concentración para soluciones). Los químicos han medido y compilado estos potenciales para una vasta gama de semirreacciones.
Para una reacción redox completa que ocurre en una pila galvánica, el potencial de celda estándar (E°_celda) se calcula de la siguiente manera:
E°_celda = E°_cátodo (potencial de reducción del electrodo donde ocurre la reducción) - E°_ánodo (potencial de reducción del electrodo donde ocurre la oxidación)
Una regla fundamental de la electroquímica establece que si el valor de E°_celda calculado es positivo (> 0 voltios), la reacción es espontánea en la dirección en que está escrita y la pila galvánica asociada puede generar energía eléctrica. Un valor negativo indica que la reacción no es espontánea en esa dirección y requeriría un aporte de energía externa para proceder. Si E°_celda es cero, el sistema se encuentra en equilibrio, y no se producirá un flujo neto de electrones ni de corriente.
Pila Galvánica vs. Celda Electrolítica: Un Contraste Esencial
Es vital diferenciar la pila galvánica de la celda electrolítica, ya que ambas implican reacciones redox pero operan bajo principios opuestos respecto a la espontaneidad y la conversión de energía. Comprender esta distinción es clave para entender cómo se aprovechan o se fuerzan las reacciones electroquímicas.
| Característica | Pila Galvánica (Redox Espontáneo) | Celda Electrolítica (Redox No Espontáneo) |
|---|---|---|
| Tipo de Reacción | Espontánea (ΔG < 0), ocurre por sí misma. | No Espontánea (ΔG > 0), requiere energía externa. |
| Conversión de Energía | Transforma energía Química → Eléctrica. | Transforma energía Eléctrica → Química. |
| Necesidad de Energía Externa | No requiere; es la fuente de energía. | Sí, requiere una fuente de alimentación externa (ej. batería, fuente de poder). |
| Polaridad del Ánodo | Negativo (fuente de electrones). | Positivo (donde se fuerza la oxidación). |
| Polaridad del Cátodo | Positivo (destino de electrones). | Negativo (donde se fuerza la reducción). |
| Flujo de Electrones | Del ánodo al cátodo (natural). | Del ánodo al cátodo (forzado por la fuente externa). |
| Aplicación Típica | Baterías, pilas, sensores químicos. | Electrodeposición (galvanoplastia), refinación de metales, producción de cloro/soda cáustica, recarga de baterías. |
Aplicaciones Cotidianas de las Reacciones Redox Espontáneas
La capacidad de las reacciones redox espontáneas para generar electricidad ha tenido un impacto profundo en nuestra sociedad, siendo la base de innumerables tecnologías que damos por sentadas. A continuación, algunas de sus aplicaciones más relevantes y su importancia:
1. Baterías y Pilas
Son quizás el ejemplo más familiar y omnipresente. Desde la pequeña pila alcalina de un solo uso que alimenta un control remoto o un juguete, hasta las sofisticadas baterías de iones de litio en nuestros smartphones, laptops y vehículos eléctricos, todas funcionan gracias a reacciones redox espontáneas. En estas baterías, se seleccionan cuidadosamente los materiales de los electrodos y los electrolitos para asegurar una reacción espontánea y eficiente que libere electrones. La diferencia principal entre una pila primaria (no recargable, como las alcalinas) y una secundaria (recargable, como las de iones de litio o plomo-ácido) es que en estas últimas, la reacción espontánea que produce electricidad puede ser revertida mediante la aplicación de energía eléctrica externa (un proceso de electrólisis), recargando la pila para usos futuros.
2. Corrosión
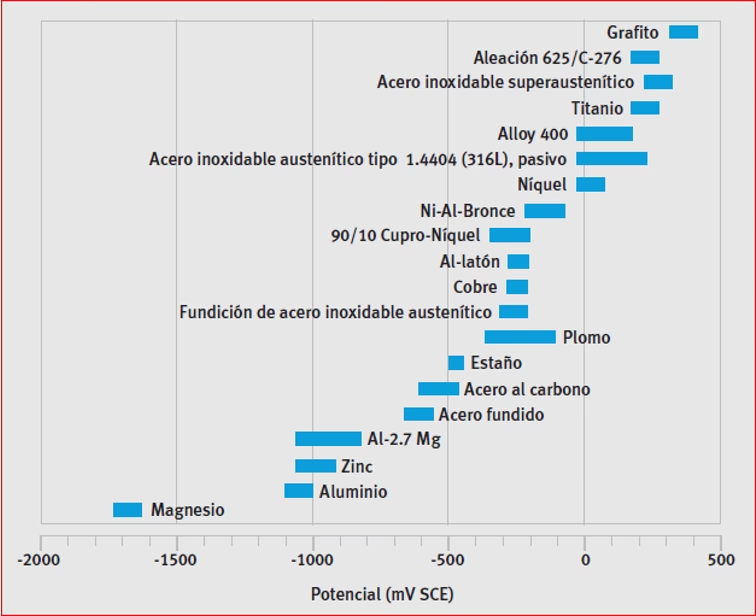
Aunque a menudo indeseable y perjudicial, la corrosión es un ejemplo clásico de una reacción redox espontánea. El óxido de hierro (herrumbre) que se forma en el acero es el resultado de la oxidación espontánea del hierro en presencia de oxígeno y agua. Este proceso libera energía, lo que explica por qué ocurre sin necesidad de intervención. Comprender los principios del redox espontáneo es crucial para desarrollar estrategias de prevención de la corrosión, como el uso de recubrimientos protectores (pinturas, galvanizado), la protección catódica (conectando el metal a proteger a un metal más reactivo) o la creación de materiales intrínsecamente resistentes como el acero inoxidable. El acero inoxidable, por ejemplo, forma una capa pasiva de óxido de cromo en su superficie que impide la continuación del proceso espontáneo de oxidación, protegiendo el metal subyacente.
3. Sensores Químicos y Dispositivos Médicos
Muchos biosensores, como los glucómetros utilizados por personas con diabetes para medir sus niveles de azúcar en sangre, utilizan reacciones redox espontáneas. Estos dispositivos contienen enzimas que catalizan una reacción redox específica con el analito (en este caso, la glucosa). La transferencia de electrones en esta reacción genera una pequeña corriente eléctrica, cuya magnitud es directamente proporcional a la concentración del analito en la muestra biológica. Esto permite una medición rápida y precisa.
Factores que Influyen en la Espontaneidad Redox
Si bien los potenciales estándar de reducción nos dan una indicación de la espontaneidad bajo condiciones ideales (estándar), en el mundo real, varios factores pueden influir en el curso, la velocidad y la magnitud de una reacción redox espontánea:
- Concentración de Reactivos y Productos: Según el principio de Le Chatelier y, más cuantitativamente, la ecuación de Nernst, las concentraciones de las especies iónicas en las semiceldas afectan el potencial de celda. Aumentar la concentración de los reactivos o disminuir la de los productos en una semirreacción puede hacer que la reacción global sea más espontánea (aumentando su potencial) o menos, si se invierten las condiciones. Las desviaciones de las concentraciones estándar alteran el ΔG de la reacción.
- Temperatura: La temperatura puede influir significativamente en la cinética de la reacción (qué tan rápido ocurre) y también en la termodinámica (la espontaneidad). La energía libre de Gibbs (ΔG) depende de la temperatura (ΔG = ΔH - TΔS). Un aumento o disminución de la temperatura puede, por lo tanto, alterar la espontaneidad de ciertas reacciones o, al menos, la magnitud de la energía liberada.
- Naturaleza de los Electrodos y Electrolitos: La elección de los materiales de los electrodos (su composición y pureza) y la composición de los electrolitos (tipo de iones, pH, fuerza iónica) son determinantes para los potenciales de celda y, por ende, para la espontaneidad, la eficiencia y la vida útil de la pila galvánica.
- Presión: Para reacciones que involucran gases, la presión parcial de los gases puede influir en la espontaneidad de manera similar a cómo lo hace la concentración para las especies en solución.
Preguntas Frecuentes (FAQs)
¿Qué es una reacción redox espontánea?
Es una reacción de oxidación-reducción que ocurre de forma natural sin necesidad de un aporte de energía externa, liberando energía en el proceso. Termodinámicamente, tiene un cambio negativo en la energía libre de Gibbs (ΔG < 0), lo que indica que es un proceso favorecido.
¿Cuál es la función principal de una pila galvánica?
La función principal de una pila galvánica es transformar la energía química liberada por una reacción redox espontánea en energía eléctrica utilizable, dirigiendo el flujo de electrones a través de un circuito externo. Esencialmente, convierte la energía de una reacción química en electricidad.
¿Por qué el puente salino es crucial en una celda galvánica?
El puente salino es crucial porque permite el flujo de iones entre las dos semiceldas, manteniendo la neutralidad de carga en las soluciones electrolíticas. Sin él, la acumulación de carga en cada semicelda detendría rápidamente el flujo de electrones y, por ende, la producción de electricidad, ya que la repulsión o atracción de cargas estáticas evitaría el movimiento continuo de electrones.
¿Cómo se diferencia una celda galvánica de una celda electrolítica?
La principal diferencia radica en la espontaneidad de la reacción y la conversión de energía. Una celda galvánica utiliza una reacción redox espontánea para generar electricidad (transformación de energía química a eléctrica). En contraste, una celda electrolítica utiliza energía eléctrica externa para forzar una reacción redox no espontánea (transformación de energía eléctrica a química).
¿Puede la corrosión ser considerada un proceso redox espontáneo?
Sí, la corrosión es un excelente ejemplo de un proceso redox espontáneo indeseable. Por ejemplo, la herrumbre del hierro ocurre cuando el hierro se oxida en presencia de oxígeno y agua, un proceso que libera energía y procede sin intervención externa. Es un proceso natural que busca un estado de menor energía.
En resumen, las reacciones redox espontáneas son la base de la electroquímica que genera energía. Desde las baterías que nos dan libertad para usar nuestros dispositivos hasta los procesos de corrosión que debemos combatir para preservar nuestras infraestructuras, entender este concepto es clave para apreciar cómo la química impulsa y moldea nuestro mundo.
Si quieres conocer otros artículos parecidos a Redox Espontáneo: Energía Química en Eléctrica puedes visitar la categoría Acero Inoxidable.